
Inflamación crónica y envejecimiento: el mecanismo silencioso del deterioro biológico
La inflamación crónica y envejecimiento están más conectados de lo que suele parecer en la práctica clínica. Más allá del paso del tiempo, el deterioro biológico puede entenderse como un proceso activo en el que participan la senescencia celular, la inmunosenescencia, la microbiota, el metabolismo y el estilo de vida.
Este enfoque ayuda a comprender por qué algunos pacientes presentan fatiga persistente, disfunción metabólica o signos de envejecimiento acelerado incluso cuando sus analíticas convencionales parecen estar dentro de la normalidad.
Autor: Redacción ESI

Los síntomas visibles pueden ser solo la superficie de procesos moleculares más profundos.
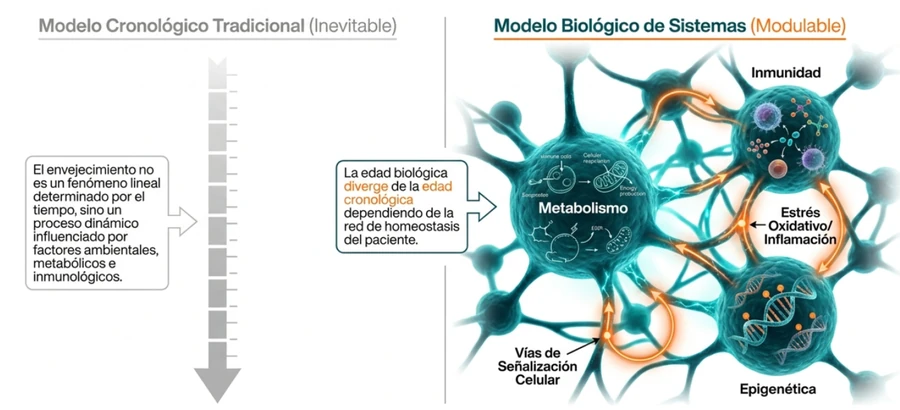
El envejecimiento no es solo desgaste: es biología activa
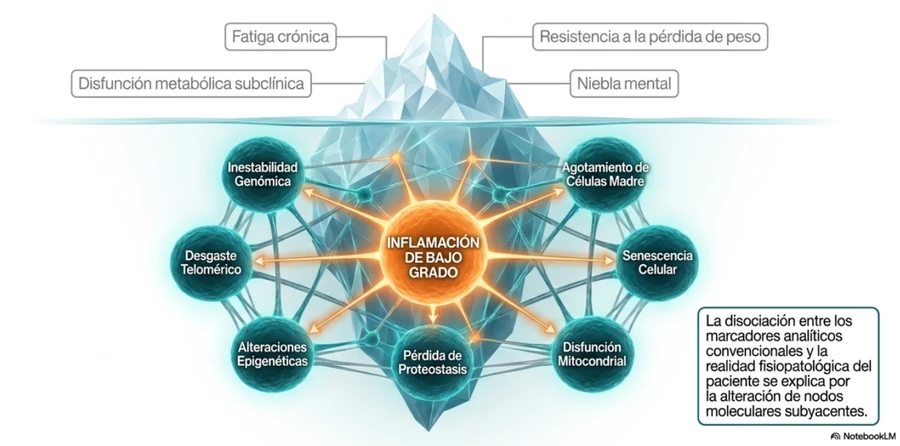
La edad biológica depende de redes de metabolismo, inmunidad, epigenética y señalización celular.
El envejecimiento suele asociarse a pérdida de fuerza, menor densidad ósea, deterioro cognitivo o reducción de la capacidad regenerativa. Estos cambios son visibles, pero detrás de ellos existen mecanismos celulares más profundos.
La célula puede responder al daño de distintas maneras. Puede reparar su función, perder su identidad especializada o entrar en un estado de senescencia. Esta última opción es especialmente relevante para comprender la relación entre inflamación crónica y envejecimiento.
Qué ocurre cuando una célula entra en senescencia
Una célula senescente deja de dividirse y pierde parte de su funcionalidad. Sin embargo, no desaparece. Permanece metabólicamente activa y puede liberar señales inflamatorias al entorno.
Por eso se las ha descrito de forma divulgativa como “células zombi”: no cumplen su función original, pero siguen influyendo en los tejidos que las rodean.
- Alteran la arquitectura del tejido.
- Favorecen la degradación de la matriz extracelular.
- Activan señales inflamatorias.
- Pueden inducir disfunción en células vecinas.
Senescencia celular e inflamación de bajo grado
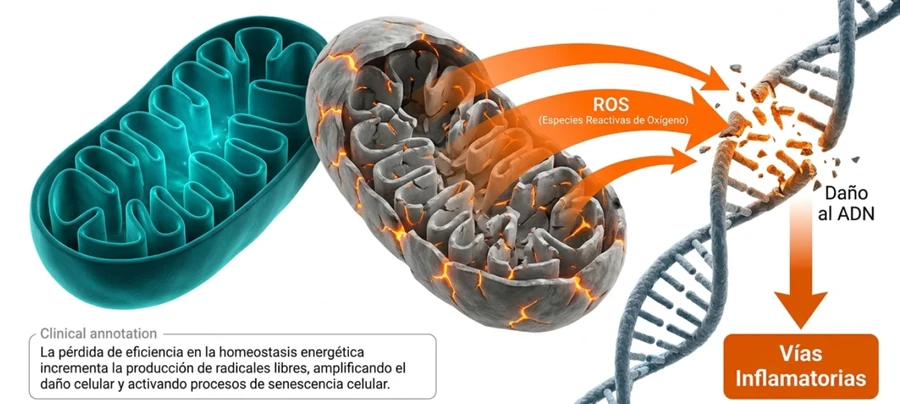
La senescencia celular puede mantener señales inflamatorias cuando falla la resolución del daño.
Las células senescentes liberan un conjunto de moléculas conocido como fenotipo secretor asociado a senescencia. Este patrón contribuye a mantener un entorno inflamatorio persistente.
Cuando el sistema inmune funciona correctamente, puede identificar y eliminar células alteradas. Pero con la edad también aparece la inmunosenescencia, es decir, una pérdida progresiva de eficacia del sistema inmunitario.
El resultado es un círculo vicioso: se acumulan células senescentes, aumenta la señalización inflamatoria y el sistema inmune envejecido tiene más dificultad para resolver el proceso.
La idea clave
La inflamación aguda es un mecanismo protector: aparece ante un daño, moviliza recursos inmunológicos y debería resolverse cuando el problema desaparece. El problema comienza cuando la respuesta inflamatoria no se apaga. En ese caso puede convertirse en una inflamación crónica de bajo grado, silenciosa y persistente, capaz de alterar la comunicación celular y contribuir al deterioro funcional. En el envejecimiento, este fenómeno se relaciona con la acumulación de células senescentes y con una menor eficacia del sistema inmune para eliminarlas. Por eso, el envejecimiento no debe entenderse solo como desgaste pasivo, sino como un proceso biológico en el que inflamación, metabolismo, microbiota, sueño, estrés y estilo de vida interactúan de forma continua.
Qué es el inflammaging
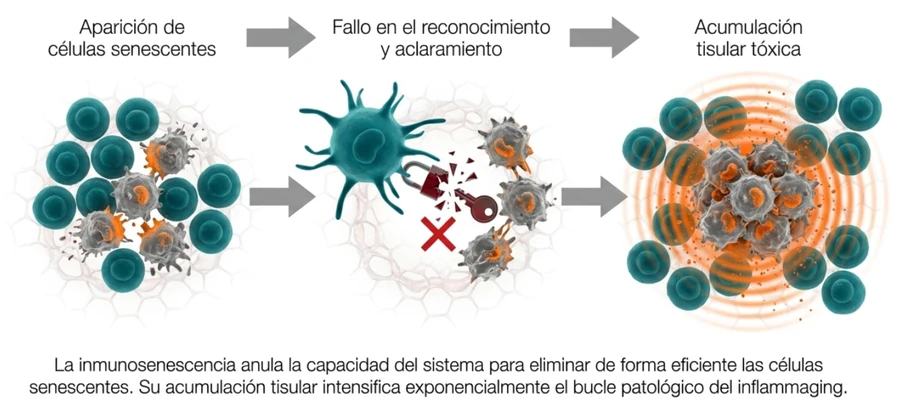
Con la edad puede disminuir la respuesta adaptativa mientras aumenta la inflamación basal.
El término inflammaging une inflamación y envejecimiento. Describe un estado de inflamación crónica de bajo grado que se desarrolla progresivamente con la edad y que puede contribuir al deterioro funcional del organismo.
Este fenómeno se caracteriza por una elevación persistente de mediadores inflamatorios, un origen multifactorial y una relación estrecha con la inmunosenescencia.
Inflamación aguda, inflamación crónica e inflamación silenciosa
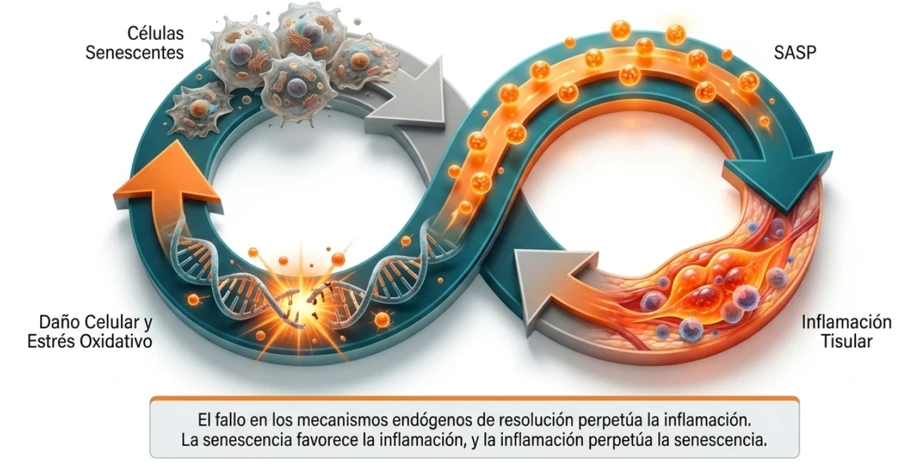
La clave clínica no es solo la inflamación, sino su duración, resolución y expresión sistémica.
No toda inflamación es negativa. La inflamación aguda es necesaria para reparar daños, responder a infecciones o iniciar procesos de recuperación. Suele ser visible: dolor, calor, enrojecimiento o hinchazón.
La inflamación crónica de bajo grado es distinta. Puede no producir dolor ni signos evidentes, pero mantenerse activa durante mucho tiempo. Por eso se la describe como una inflamación silenciosa.
Relación con enfermedades crónicas
La inflamación crónica de bajo grado se ha relacionado con múltiples enfermedades crónicas no transmisibles. Entre ellas se mencionan enfermedades cardiovasculares, diabetes, enfermedades neurodegenerativas, osteoartritis, fibrosis, procesos metabólicos alterados y deterioro funcional asociado a la edad.
Desde esta perspectiva, la inflamación no es un fenómeno aislado, sino un denominador común que puede participar en distintos procesos fisiopatológicos.
Más allá de la obesidad: metainflamación y estilo de vida
La grasa visceral es una fuente importante de inflamación crónica de bajo grado. Sin embargo, reducir todo el problema a la obesidad sería insuficiente.
El enfoque más amplio es el de la metainflamación: una inflamación relacionada con alteraciones metabólicas, estilo de vida, sedentarismo, estrés, sueño, alimentación, exposición a tóxicos y microbiota.
Factores que pueden alimentar la inflamación crónica
- Patrones alimentarios de baja calidad nutricional.
- Sedentarismo y pérdida de masa muscular.
- Estrés psicológico crónico.
- Alteración de los ritmos circadianos.
- Disbiosis intestinal o hiperpermeabilidad.
- Exposición acumulada a tóxicos ambientales.
Microbiota, intestino e inflamación sistémica
La microbiota intestinal tiene un papel central en la regulación inmunológica. Cuando existe disbiosis o alteración de la barrera intestinal, algunas moléculas de origen microbiano pueden entrar en contacto con el sistema inmune y favorecer señales inflamatorias.
Este punto conecta directamente con uno de los ejes clínicos más relevantes: salud intestinal, microbiota e inflamación sistémica no pueden entenderse como compartimentos separados.
Desde esta perspectiva, la salud intestinal actúa como un punto de conexión entre microbiota, barrera intestinal, inmunidad e inflamación sistémica.
Nutrición, ejercicio, estrés y sueño
El abordaje de la inflamación crónica no se basa en una única intervención. Requiere una lectura integrada del paciente y de sus determinantes de salud.
Nutrición
Nutrición y ejercicio pueden actuar sobre vías reguladoras implicadas en inflamación y función mitocondrial.
La alimentación puede modular la inflamación, el metabolismo y la microbiota. En el contenido fuente se destaca la importancia de una dieta con densidad nutritiva, bajo impacto glucémico, buena calidad de grasas, presencia de fitonutrientes y apoyo a la salud intestinal.
Ejercicio físico
El ejercicio influye sobre músculo, corazón, cerebro, pulmones y metabolismo. La pérdida de masa y potencia muscular puede participar en el deterioro funcional y en el estado inflamatorio asociado a la edad.
Estrés
El estrés agudo es adaptativo. El problema aparece cuando se mantiene de forma crónica. En ese contexto puede alterar la respuesta inmunitaria y favorecer un entorno proinflamatorio.
Sueño y ritmos circadianos
La alteración de los ciclos sueño-vigilia se relaciona con regulación hormonal, función inmune y relojes biológicos. Por ello, los ritmos circadianos forman parte del mapa clínico de la inflamación crónica y envejecimiento.
Tabla práctica para consulta
| Perfil | Hipótesis clínica | Qué priorizar | Señales de mejora |
|---|---|---|---|
| Paciente con fatiga persistente | Inflamación silenciosa, estrés crónico o disfunción metabólica | Sueño, estrés, alimentación, actividad física progresiva | Más energía, mejor descanso, menor sensación de agotamiento |
| Paciente con grasa visceral | Metainflamación y resistencia metabólica | Composición corporal, nutrición, ejercicio de fuerza y aeróbico | Mejor perímetro abdominal, más fuerza, mejor control metabólico |
| Paciente con disbiosis o síntomas digestivos | Activación inmune desde el eje intestinal | Microbiota, barrera intestinal, tolerancia alimentaria | Mejor digestión, menor hinchazón, mayor regularidad intestinal |
| Paciente con envejecimiento funcional acelerado | Senescencia celular, inmunosenescencia y baja reserva funcional | Movimiento, nutrición, sueño, inflamación de bajo grado | Más autonomía, mejor capacidad física, menor fragilidad |
Mini casos clínicos hipotéticos
Caso 1: fatiga y analíticas convencionales normales
Una paciente de mediana edad consulta por cansancio mantenido, sueño poco reparador y dificultad para recuperar tras jornadas exigentes. Sus pruebas convencionales no muestran alteraciones relevantes. Desde una lectura integrativa, podría explorarse la presencia de inflamación de bajo grado, estrés crónico, alteración circadiana y salud intestinal.
Caso 2: deterioro funcional progresivo
Un paciente mayor refiere pérdida de fuerza, menor tolerancia al ejercicio y aumento de perímetro abdominal. En este caso, el foco no estaría solo en el peso, sino en composición corporal, potencia muscular, metainflamación, patrón alimentario y calidad del descanso.
Cómo aplicarlo mañana en consulta
Una forma práctica de trasladar este modelo a la consulta es dejar de buscar una única causa lineal y empezar a mapear factores interconectados. Ante fatiga, deterioro funcional, grasa visceral, disbiosis, sueño alterado o estrés crónico, puede ser útil valorar si existe un terreno de inflamación crónica de bajo grado. Esto no implica sustituir el diagnóstico médico ni indicar tratamientos sin criterio, sino ampliar la anamnesis: alimentación, ejercicio, composición corporal, ritmo sueño-vigilia, estrés, síntomas digestivos, exposición a tóxicos y evolución funcional. El objetivo clínico no es “apagar” la inflamación de forma inespecífica, sino favorecer condiciones de resolución: mejor nutrición, mejor descanso, más movimiento, mejor regulación del estrés y una microbiota más equilibrada.
Preguntas frecuentes
¿Qué relación hay entre inflamación crónica y envejecimiento?
La inflamación crónica de bajo grado puede contribuir al deterioro funcional asociado a la edad. Se relaciona con senescencia celular, inmunosenescencia y alteraciones metabólicas que pueden favorecer un envejecimiento menos saludable.
¿El inflammaging es lo mismo que inflamación aguda?
No. La inflamación aguda es una respuesta reparadora y temporal. El inflammaging hace referencia a una inflamación crónica, silenciosa y persistente asociada al proceso de envejecimiento.
¿La obesidad explica toda la inflamación crónica?
No. La grasa visceral es relevante, pero la inflamación crónica también puede relacionarse con alimentación, sedentarismo, estrés, sueño, microbiota, tóxicos y otros factores del estilo de vida.
¿La microbiota puede influir en el envejecimiento?
Según el enfoque expuesto, la microbiota puede participar en la regulación inmunológica. La disbiosis o la alteración de la barrera intestinal pueden favorecer señales inflamatorias sistémicas.
¿Qué papel tiene el ejercicio?
El ejercicio contribuye a preservar masa muscular, función metabólica y capacidad funcional. También se relaciona con mecanismos que pueden modular la inflamación y el envejecimiento biológico.
¿El estrés crónico acelera el envejecimiento?
El estrés agudo es adaptativo, pero el estrés crónico puede alterar la regulación inmunitaria y favorecer un entorno proinflamatorio mantenido.
¿Tiene sentido usar antiinflamatorios convencionales?
El contenido fuente diferencia la inflamación aguda de la inflamación crónica de bajo grado. En esta última, el enfoque no debería centrarse solo en suprimir, sino en favorecer mecanismos de resolución y abordar factores de base.
Checklist final para valorar inflamación crónica y envejecimiento
- Explorar fatiga persistente y capacidad de recuperación.
- Valorar composición corporal, especialmente grasa visceral y masa muscular.
- Revisar patrón alimentario y densidad nutricional.
- Investigar síntomas digestivos compatibles con disbiosis.
- Preguntar por sueño, horarios y ritmos circadianos.
- Evaluar nivel de sedentarismo y ejercicio de fuerza.
- Identificar estrés crónico y carga psicoemocional.
- Considerar exposición a tóxicos ambientales o laborales.
- Revisar marcadores inflamatorios cuando proceda.
- Observar pérdida de fuerza, potencia o autonomía.
- Valorar antecedentes metabólicos y cardiovasculares.
- Evitar enfoques lineales ante problemas multifactoriales.
- Priorizar estrategias de resolución, no solo de supresión.
- Integrar nutrición, microbiota, movimiento, sueño y estrés.
- Personalizar el abordaje según el perfil del paciente.
Conclusión
La inflamación crónica y envejecimiento forman parte de un mismo mapa biológico. El deterioro asociado a la edad no depende únicamente del calendario, sino de procesos celulares, inmunológicos, metabólicos y ambientales que se acumulan con el tiempo.
Desde una perspectiva integrativa, el reto consiste en identificar los factores que mantienen la inflamación silenciosa y favorecer condiciones de resolución: nutrición adecuada, actividad física, equilibrio circadiano, regulación del estrés y salud intestinal.
El objetivo no es prometer una vida más larga, sino comprender mejor cómo preservar función, autonomía y calidad de vida a lo largo del proceso de envejecimiento.
Referencias bibliográficas
Bibliografía científica
Evidencia mecanística
- López-Otín C, Blasco MA, Partridge L, Serrano M, Kroemer G. Hallmarks of aging: An expanding universe. Cell. 2023;186(2):243-278. doi:10.1016/j.cell.2022.11.001. PMID: 36599349.
- Franceschi C, Campisi J. Chronic inflammation (inflammaging) and its potential contribution to age-associated diseases. J Gerontol A Biol Sci Med Sci. 2014;69 Suppl 1:S4-S9. doi:10.1093/gerona/glu057. PMID: 24833586.
- Franceschi C, Garagnani P, Parini P, Giuliani C, Santoro A. Inflammaging: a new immune-metabolic viewpoint for age-related diseases. Nat Rev Endocrinol. 2018;14(10):576-590. doi:10.1038/s41574-018-0059-4. PMID: 30046148.
- Tchkonia T, Zhu Y, van Deursen J, Campisi J, Kirkland JL. Cellular senescence and the senescent secretory phenotype: therapeutic opportunities. J Clin Invest. 2013;123(3):966-972. doi:10.1172/JCI64098. PMID: 23454759.
- Zhang L, Pitcher LE, Yousefzadeh MJ, Niedernhofer LJ, Robbins PD, Zhu Y. Cellular senescence: a key therapeutic target in aging and diseases. J Clin Invest. 2022;132(15):e158450. doi:10.1172/JCI158450. PMID: 35912854.
- Santoro A, Bientinesi E, Monti D. Immunosenescence and inflammaging in the aging process: age-related diseases or longevity? Ageing Res Rev. 2021;71:101422. doi:10.1016/j.arr.2021.101422. PMID: 34391943.
Evidencia clínica
- Conway J, Duggal NA. Ageing of the gut microbiome: potential influences on immune senescence and inflammageing. Ageing Res Rev. 2021;68:101323. doi:10.1016/j.arr.2021.101323. PMID: 33771720.
- Bosco N, Noti M. The aging gut microbiome and its impact on host immunity. Genes Immun. 2021;22(5-6):289-303. doi:10.1038/s41435-021-00126-8.
- Koelman L, Egea Rodrigues C, Aleksandrova K. Effects of dietary patterns on biomarkers of inflammation and immune responses: a systematic review and meta-analysis of randomized controlled trials. Adv Nutr. 2022;13(1):101-115. doi:10.1093/advances/nmab086. PMID: 34607347.
- Khalafi M, Akbari A, Symonds ME, Pourvaghar MJ, Rosenkranz SK, Tabari E. Influence of different modes of exercise training on inflammatory markers in older adults with and without chronic diseases: a systematic review and meta-analysis. Cytokine. 2023;169:156303. doi:10.1016/j.cyto.2023.156303. PMID: 37467710.
- Irwin MR, Olmstead R, Carroll JE. Sleep disturbance, sleep duration, and inflammation: a systematic review and meta-analysis of cohort studies and experimental sleep deprivation. Biol Psychiatry. 2016;80(1):40-52. doi:10.1016/j.biopsych.2015.05.014. PMID: 26140821.
- Garbarino S, Lanteri P, Bragazzi NL, Magnavita N, Scoditti E. Role of sleep deprivation in immune-related disease risk and outcomes. Commun Biol. 2021;4:1304. doi:10.1038/s42003-021-02825-4.
Seguridad
- Berger MM, Shenkin A, Schweinlin A, et al. ESPEN micronutrient guideline. Clin Nutr. 2022;41(6):1357-1424. doi:10.1016/j.clnu.2022.02.015. PMID: 35365361. Evidencia aplicable a la prudencia en suplementación y evaluación individualizada.
- Volkert D, Beck AM, Cederholm T, et al. ESPEN guideline on clinical nutrition and hydration in geriatrics. Clin Nutr. 2019;38(1):10-47. doi:10.1016/j.clnu.2018.05.024. Evidencia aplicable a nutrición, envejecimiento y preservación funcional.
Posición de organismos oficiales, guías y consensos
- Bull FC, Al-Ansari SS, Biddle S, et al. World Health Organization 2020 guidelines on physical activity and sedentary behaviour. Br J Sports Med. 2020;54(24):1451-1462. doi:10.1136/bjsports-2020-102955. PMID: 33239350.
- Watson NF, Badr MS, Belenky G, et al. Recommended amount of sleep for a healthy adult: a joint consensus statement of the American Academy of Sleep Medicine and Sleep Research Society. Sleep. 2015;38(6):843-844. doi:10.5665/sleep.4716.
- Visseren FLJ, Mach F, Smulders YM, et al. 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice. Eur Heart J. 2021;42(34):3227-3337. doi:10.1093/eurheartj/ehab484. PMID: 34458905.
Controversias o límites del conocimiento
- Conway J, Duggal NA. Ageing of the gut microbiome: potential influences on immune senescence and inflammageing. Ageing Res Rev. 2021;68:101323. doi:10.1016/j.arr.2021.101323. PMID: 33771720. Aunque la relación microbiota-inflamación-envejecimiento es plausible, la causalidad clínica y la respuesta individual siguen siendo áreas en desarrollo.
- Zhang L, Pitcher LE, Yousefzadeh MJ, Niedernhofer LJ, Robbins PD, Zhu Y. Cellular senescence: a key therapeutic target in aging and diseases. J Clin Invest. 2022;132(15):e158450. doi:10.1172/JCI158450. PMID: 35912854. La investigación sobre senolíticos y senomórficos es prometedora, pero su aplicación clínica generalizada requiere más ensayos en humanos y evaluación de seguridad.
- Irwin MR, Olmstead R, Carroll JE. Sleep disturbance, sleep duration, and inflammation: a systematic review and meta-analysis of cohort studies and experimental sleep deprivation. Biol Psychiatry. 2016;80(1):40-52. doi:10.1016/j.biopsych.2015.05.014. PMID: 26140821. La evidencia apoya asociación entre sueño e inflamación, aunque existen diferencias según duración, calidad del sueño, población estudiada y biomarcadores analizados.
¿Quieres saber más?
Echa un vistazo a nuestras formaciones relacionadas con el tema de este artículo:






