Probióticos, prebióticos y posbióticos en la práctica clínica: una guía integrativa basada en evidencia
Los probióticos, prebióticos y posbióticos en la práctica clínica han pasado de ser un tema periférico a ocupar un lugar central en la conversación sobre microbiota, nutrición y medicina integrativa. El crecimiento de la literatura científica obliga a ir más allá de los mensajes simplificados y a comprender cómo seleccionar, combinar e indicar estas herramientas con criterio clínico. No se trata de “añadir bacterias” de forma inespecífica, sino de intervenir sobre un ecosistema complejo con objetivos concretos.
Autor: Redacción ESI
Por qué hablar hoy de “bióticos” exige más precisión clínica
El término “bióticos” engloba varias categorías con definiciones, mecanismos y aplicaciones diferentes. En consulta, confundirlas puede traducirse en expectativas irreales, elecciones poco ajustadas al contexto del paciente o uso de productos mal caracterizados.
La visión actual del microbioma ya no se limita a describir qué microorganismos están presentes. También importa qué funciones desempeñan, cómo interactúan entre sí, qué metabolitos producen y cómo se relacionan con la barrera intestinal, el sistema inmune y otros ejes fisiológicos relevantes.
Desde la perspectiva de ESI, este campo conecta de forma natural con tres grandes áreas: nutrición, suplementación y microbiota. Por eso, una buena estrategia clínica necesita integrar dieta, contexto digestivo, tolerancia individual y objetivo terapéutico.
Probióticos: la selección de cepas importa más que la etiqueta general
La definición de referencia establece que los probióticos son microorganismos vivos que, administrados en cantidades adecuadas, confieren un beneficio a la salud del huésped. Esta formulación, ampliamente aceptada en el ámbito científico, tiene implicaciones prácticas inmediatas: no basta con saber el género o la especie; la cepa concreta es la unidad relevante de evidencia.
Qué debe revisar un profesional antes de indicar un probiótico
- Género, especie y cepa claramente identificados en etiquetado o ficha técnica.
- Indicación concreta respaldada por revisiones, metaanálisis o guías cuando existan.
- Dosis utilizada en estudios, evitando extrapolaciones genéricas.
- Calidad y estabilidad del producto durante su vida útil.
- Contexto clínico: antibioterapia, fragilidad digestiva, intolerancia fermentativa o inmunocompromiso.
Este enfoque evita uno de los errores más frecuentes: asumir que todas las cepas de una misma especie comparten los mismos efectos. En microbiota clínica, esa extrapolación no es segura. Si el producto no especifica la cepa, disminuye de forma importante la capacidad del profesional para anticipar su comportamiento.
Mitos frecuentes sobre UFC y colonización
Otro punto de confusión es la idea de que más Unidades Formadoras de Colonias siempre significan mayor eficacia. En realidad, la dosis útil depende de la cepa, de la indicación y del escenario clínico. No existe una equivalencia automática entre “más cantidad” y “mejor resultado”.
Tampoco es imprescindible que un probiótico colonice de forma estable el intestino para ser clínicamente relevante. Algunas cepas ejercen efectos transitorios sobre la microbiota residente, la inmunidad mucosal o la función de barrera, y aun así pueden resultar útiles en momentos concretos, como tras una exposición a antibióticos.
Prebióticos: no toda fibra actúa igual sobre la microbiota
Los prebióticos se definen como sustratos utilizados de forma selectiva por los microorganismos del hospedador que confieren un beneficio para la salud. Esta definición obliga a distinguir entre fibra dietética general y compuestos con una acción selectiva sobre grupos microbianos o funciones concretas.
Prebióticos relevantes en la práctica clínica
- Inulina y fructooligosacáridos (FOS): compuestos muy fermentables, útiles en determinados contextos, aunque no siempre bien tolerados.
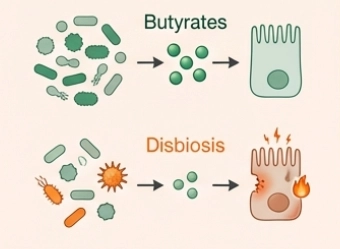
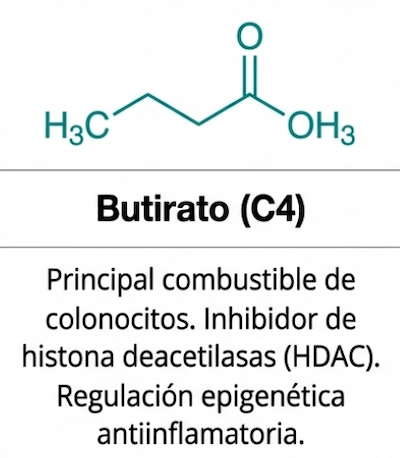
- Almidón resistente: de especial interés por su relación con la producción de ácidos grasos de cadena corta y el soporte a bacterias beneficiosas.
- Betaglucanos: presentes en algunas fuentes vegetales, hongos y algas, con interés en inmunomodulación.
- HMO u oligosacáridos de la leche materna: referencia biológica destacada por su complejidad y selectividad funcional.
El hecho de que un prebiótico sea potencialmente beneficioso no implica que sea universalmente bien tolerado. En pacientes con distensión, dolor, fermentación excesiva o sospecha de sobrecrecimiento bacteriano, aumentar sustratos fermentables sin valorar el contexto puede empeorar la clínica. La clave no es solo “dar fibra”, sino decidir qué sustrato, cuándo y en qué dosis.
La idea clave
La intervención sobre la microbiota no debería abordarse como una reposición mecánica de microorganismos “buenos”, sino como una modulación estratégica de un ecosistema dinámico. Un probiótico no se elige por popularidad ni por número de UFC, sino por la evidencia asociada a una cepa concreta, la dosis estudiada y la adecuación al perfil clínico. Un prebiótico tampoco se indica por el simple hecho de ser fibra: debe valorarse si el paciente puede tolerarlo, si el contexto digestivo favorece su uso y qué función se quiere estimular.
Los posbióticos amplían aún más este marco, al permitir trabajar con componentes microbianos inanimados cuando interesa una señalización específica sin necesidad de microorganismos viables. En conjunto, el mensaje clínico de fondo es claro: no existen “bióticos” universales. Existen herramientas distintas para escenarios distintos. La buena práctica consiste en identificar el patrón disbiótico probable, los objetivos prioritarios y la intervención mejor alineada con ese contexto, integrando alimentación, fisiología digestiva, tolerancia individual y seguimiento evolutivo.
Simbióticos: cuándo la combinación tiene sentido clínico
Los simbióticos combinan microorganismos vivos y sustratos con la intención de generar un beneficio conjunto. Sin embargo, no todas las combinaciones responden a la misma lógica.
Dos categorías útiles para interpretar un simbiótico
1. Simbióticos complementarios
Reúnen un probiótico y un prebiótico con beneficios potenciales propios, aunque el sustrato no esté diseñado específicamente para alimentar a la cepa acompañante.
2. Simbióticos sinérgicos
Buscan una interacción más dirigida: el sustrato se selecciona expresamente para favorecer el crecimiento o la actividad del microorganismo administrado.
Esta distinción es útil al valorar fórmulas complejas. Una combinación extensa no es necesariamente mejor; lo relevante es si existe una lógica fisiológica y clínica detrás de su diseño.
Posbióticos: señalización sin viabilidad
Los posbióticos representan una de las áreas más interesantes de la evolución conceptual del campo. Se entienden como preparaciones de microorganismos inanimados y/o sus componentes que confieren un beneficio a la salud. Aquí pueden incluirse células inactivadas, fragmentos estructurales y otros elementos capaces de interactuar con el huésped.
Su interés práctico radica en que permiten aprovechar determinados efectos biológicos sin depender de la viabilidad del microorganismo. Esto puede resultar especialmente relevante cuando no se busca colonización, cuando la seguridad o la estabilidad son consideraciones prioritarias, o cuando el efecto de interés deriva de la estructura microbiana y no de su actividad metabólica completa.
También conviene mantener precisión terminológica: un metabolito aislado, como el butirato purificado, no equivale automáticamente a un posbiótico en sentido técnico estricto.
Mecanismos de acción en la microbiota clínica: del lumen intestinal al eje sistémico
Los bióticos pueden actuar en varios niveles, y esa visión multinivel ayuda a seleccionar mejor la intervención.
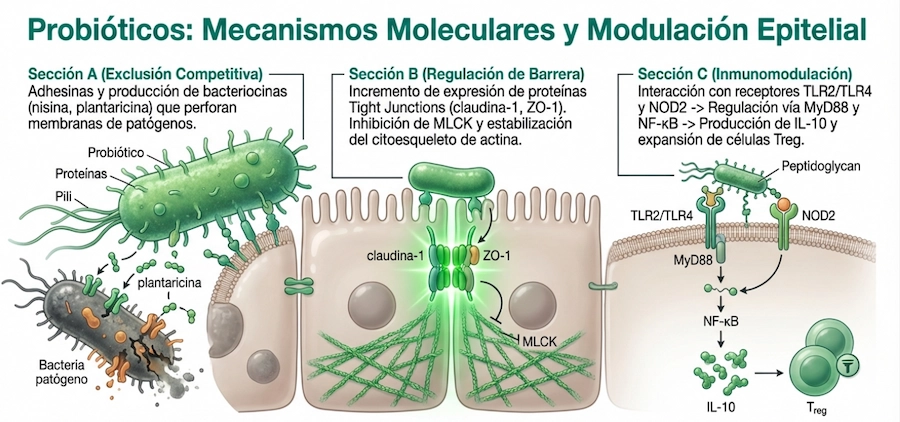
Nivel 1: lumen intestinal
Incluye la competencia con microorganismos potencialmente problemáticos, la producción de bacteriocinas y la modificación del entorno luminal.
Nivel 2: mucosa y epitelio
Se relaciona con la integridad de barrera, la producción de mucina y la modulación del sistema inmune asociado a mucosas, incluida la respuesta secretora.
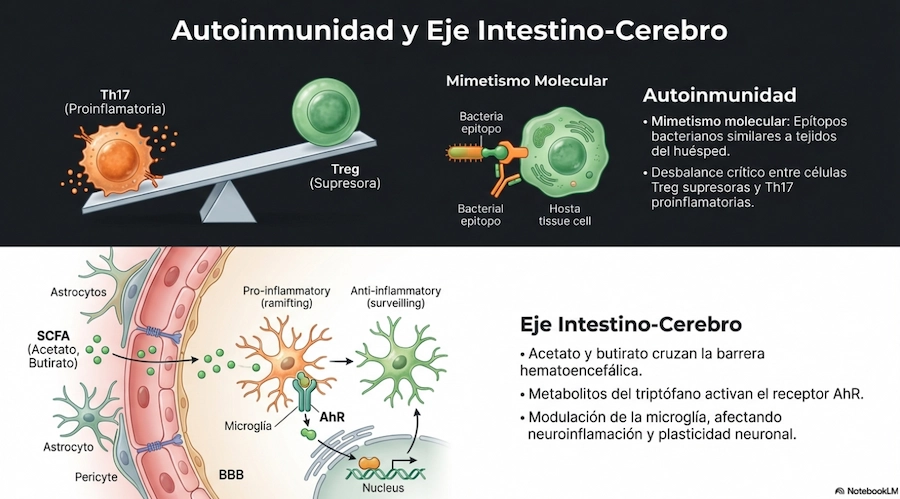
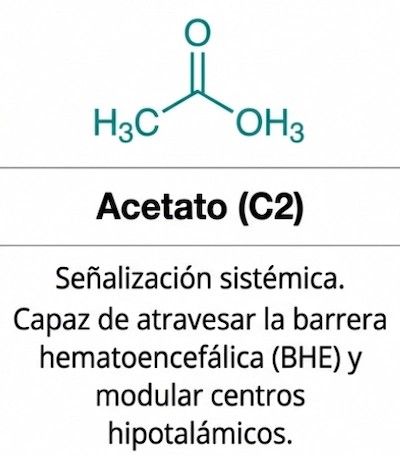
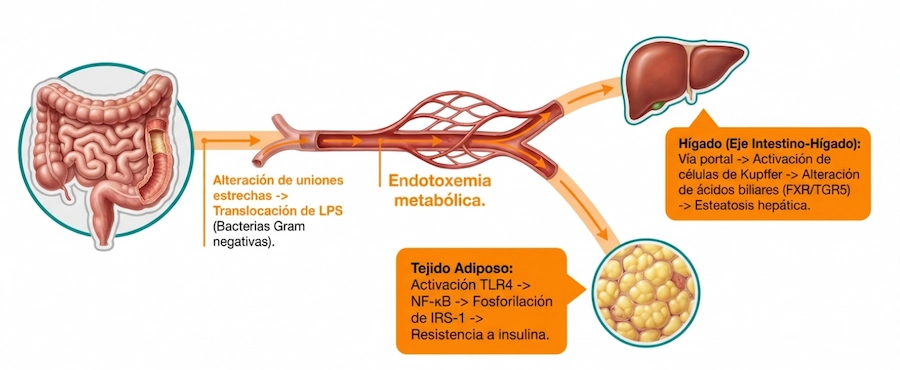
Nivel 3: efectos sistémicos
Comprende la señalización más allá del intestino, con impacto potencial sobre inflamación, inmunidad sistémica y comunicación intestino-cerebro.
Cross-feeding: una idea central para no simplificar
La alimentación cruzada o cross-feeding recuerda que, al introducir una cepa o un sustrato, no solo se modifica su diana directa. También pueden verse favorecidas otras especies residentes mediante metabolitos intermedios o interacciones cooperativas. Esto es especialmente importante al diseñar estrategias escalonadas y al interpretar respuestas clínicas no lineales.
Cómo aplicarlo mañana en consulta
Ante un paciente con sospecha de disbiosis, el primer paso útil no suele ser escoger un producto, sino formular una hipótesis funcional. ¿Predomina la intolerancia fermentativa? ¿Hay antecedente reciente de antibióticos? ¿La prioridad es la barrera intestinal, la regularidad, la tolerancia digestiva o la modulación inmune? A partir de ahí, la intervención puede ordenarse mejor.
En términos prácticos, conviene revisar la dieta de base, valorar la tolerancia a fibras fermentables, identificar si existe una indicación clara para una cepa concreta y considerar si el escenario favorece un probiótico, un prebiótico, un simbiótico o un posbiótico. Después, el seguimiento debe centrarse en marcadores clínicos realistas: síntomas digestivos, patrón de deposición, tolerancia, percepción de hinchazón, evolución de la regularidad o necesidad de reajuste. Esta lógica evita el uso indiscriminado de fórmulas amplias y ayuda a convertir la microbiota en una herramienta clínica más precisa y menos basada en inercias comerciales.
Tabla práctica de orientación clínica
| Perfil | Hipótesis clínica | Qué priorizar | Señales de mejora |
|---|---|---|---|
| Paciente tras antibioterapia | Alteración transitoria del ecosistema y de la función barrera | Selección de cepa con evidencia en ese contexto y vigilancia de tolerancia | Mejor patrón digestivo, menos distensión, recuperación de regularidad |
| Paciente con baja tolerancia fermentativa | Exceso de fermentación o sensibilidad a ciertos sustratos | Introducción prudente de prebióticos o elección de estrategias no fermentativas | Reducción de gases, dolor y sensación de pesadez |
| Paciente con objetivo de soporte mucosal | Compromiso funcional de la barrera intestinal | Intervención combinada: nutrición, microbiota y seguimiento clínico | Menor reactividad digestiva y mejor tolerancia alimentaria |
| Paciente con intervención nutricional incompleta | Base dietética insuficiente para sostener cambios en microbiota | Corregir primero sustrato dietético y calidad de la alimentación | Mayor estabilidad digestiva y mejor respuesta a suplementos |
Mini casos clínicos hipotéticos
Caso 1
Profesional sanitaria de 42 años, sin patología orgánica conocida, consulta por hinchazón y cambios del ritmo intestinal tras un ciclo reciente de antibióticos. Refiere buena alimentación general, pero baja tolerancia a alimentos muy fermentables desde entonces. La hipótesis clínica prioriza una alteración transitoria del ecosistema intestinal y de la tolerancia mucosal. En este escenario, puede ser más razonable comenzar con una estrategia prudente, evitando aumentar de entrada sustratos altamente fermentables y valorando una cepa concreta con evidencia en recuperación postantibiótica, junto con seguimiento de síntomas.
Caso 2
Varón de 55 años con estreñimiento funcional, dieta pobre en variedad vegetal y elevado estrés laboral. El objetivo inicial no sería solo indicar un probiótico, sino reconstruir el terreno: mejorar la base alimentaria, revisar ingesta de carbohidratos accesibles a la microbiota y plantear un prebiótico o simbiótico según tolerancia. La señal de progreso no dependería de una analítica aislada, sino de variables clínicas sencillas: regularidad, confort abdominal, menor distensión y mejor tolerancia digestiva.
FAQ: dudas frecuentes sobre bióticos y microbiota clínica
¿Todos los probióticos sirven para lo mismo?
No. La evidencia se estudia a nivel de cepa y contexto clínico. Dos productos con nombres parecidos pueden tener perfiles muy diferentes si no comparten la misma identificación microbiológica ni la misma base de estudios.
¿La frase “más UFC” implica más eficacia?
No necesariamente. En probióticos, prebióticos y posbióticos en la práctica clínica, la dosis debe interpretarse en función de la cepa, la indicación y la tolerancia del paciente. Más cantidad no equivale automáticamente a mejor respuesta.
¿Un probiótico debe colonizar el intestino para resultar útil?
No siempre. Algunas cepas ejercen efectos transitorios sobre el entorno intestinal, la barrera o la inmunidad mucosal sin establecer una colonización permanente. Ese efecto temporal puede ser clínicamente relevante.
¿Un prebiótico es simplemente cualquier fibra?
No. Un prebiótico debe ser utilizado de forma selectiva por microorganismos del hospedador y asociarse a un beneficio para la salud. Por eso no toda fibra dietética cumple la definición técnica.
¿Cuándo conviene extremar la prudencia con prebióticos?
Especialmente cuando existe mala tolerancia fermentativa, distensión importante o sospecha de sobrecrecimiento bacteriano. En esos casos, aumentar ciertos sustratos sin estrategia puede empeorar la sintomatología.
¿Qué aporta un posbiótico frente a un probiótico?
Puede aportar señalización biológica sin necesidad de microorganismos viables. Esto resulta interesante cuando la prioridad es un efecto estructural o inmunológico y no una interacción basada en viabilidad o colonización transitoria.
¿Cómo se integran los bióticos en medicina integrativa?
Siempre dentro de una visión más amplia que incluya dieta, función digestiva, estado inflamatorio, tolerancia individual y objetivo terapéutico. En probióticos, prebióticos y posbióticos en la práctica clínica, el suplemento aislado rara vez sustituye a una estrategia bien construida.
Checklist final para una indicación más precisa
- Definir el objetivo clínico antes de elegir el producto.
- Comprobar si el producto identifica género, especie y cepa.
- Revisar si la indicación se apoya en revisiones, guías o metaanálisis.
- Valorar la dieta de base antes de suplementar.
- Explorar tolerancia a fibras fermentables.
- Distinguir entre necesidad de probiótico, prebiótico, simbiótico o posbiótico.
- Evitar extrapolar datos de una cepa a toda una especie.
- No usar las UFC como único criterio de calidad.
- Tener en cuenta antecedentes de antibioterapia reciente.
- Considerar la función barrera como objetivo clínico específico.
- Empezar de forma prudente si existe distensión o fermentación excesiva.
- Monitorizar cambios clínicos sencillos y relevantes.
- Reajustar según respuesta, no según expectativas teóricas.
- Integrar microbiota, nutrición y suplementación en un mismo plan.
Conclusión
El campo de los bióticos ha madurado lo suficiente como para exigir un lenguaje clínico más fino y una selección más cuidadosa. Probióticos, prebióticos, simbióticos y posbióticos no son conceptos intercambiables, sino herramientas con funciones diferentes dentro de una misma ecología intestinal. La práctica clínica más útil será aquella capaz de individualizar, evitar simplificaciones y construir estrategias coherentes con el terreno fisiológico y nutricional de cada paciente.
Referencias bibliográficas
Bibliografía científica
Las referencias siguientes se han seleccionado para respaldar de forma trazable las definiciones, mecanismos, aplicaciones clínicas, aspectos de seguridad y límites de interpretación expuestos en el artículo. Se priorizan consensos de sociedades científicas, guías, revisiones sistemáticas, metaanálisis y ensayos clínicos relevantes en humanos.
Evidencia mecanística
- Zheng Y, Zhang Z, Tang P, Wu Y, Zhang A, Li D, et al. Probiotics fortify intestinal barrier function: a systematic review and meta-analysis of randomized trials. Front Immunol. 2023;14:1143548.
doi:10.3389/fimmu.2023.1143548.
PMID: 37168869.Nivel de evidencia: revisión sistemática y metaanálisis de ECA.Aplica a: barrera intestinal, mucosa, inflamación, bloque citable 1, tabla y checklist.Limitaciones: heterogeneidad entre cepas, dosis, poblaciones y biomarcadores de permeabilidad. - Ríos-Covián D, Gueimonde M, Duncan SH, Flint HJ, de los Reyes-Gavilán CG. Enhanced butyrate formation by cross-feeding between Faecalibacterium prausnitzii and Bifidobacterium adolescentis. FEMS Microbiol Lett. 2015;362(21):fnv176.
doi:10.1093/femsle/fnv176.
PMID: 26420851.Nivel de evidencia: estudio mecanístico experimental.Aplica a: cross-feeding y razonamiento ecológico del microbioma.Limitaciones: modelo experimental; no permite extrapolación clínica directa. - Moens F, Weckx S, De Vuyst L. Bifidobacterial inulin-type fructan degradation capacity determines cross-feeding interactions between bifidobacteria and Faecalibacterium prausnitzii. Int J Food Microbiol. 2016;231:76-85.
doi:10.1016/j.ijfoodmicro.2016.05.015.
PMID: 27233082.Nivel de evidencia: estudio mecanístico experimental.Aplica a: prebióticos, almidón/inulina, alimentación cruzada y ecología microbiana.Limitaciones: evidencia in vitro; utilidad principal para interpretar mecanismos. - Zheng J, Wittouck S, Salvetti E, Franz CMAP, Harris HMB, Mattarelli P, et al. A taxonomic note on the genus Lactobacillus: Description of 23 novel genera, emended description of the genus Lactobacillus Beijerinck 1901, and union of Lactobacillaceae and Leuconostocaceae. Int J Syst Evol Microbiol. 2020;70(4):2782-2858.
doi:10.1099/ijsem.0.004107.
PMID: 32293557.Nivel de evidencia: consenso taxonómico/microbiológico.Aplica a: actualización de nomenclatura y selección precisa de cepas.Limitaciones: no es evidencia de eficacia clínica; respalda terminología y trazabilidad.
Evidencia clínica
- Goodman C, Keating GM, Georgousopoulou EN, Levett K. Probiotics for the prevention of antibiotic-associated diarrhoea: a systematic review and meta-analysis. BMJ Open. 2021;11(8):e043054.
doi:10.1136/bmjopen-2020-043054.
PMID: 34385227.Nivel de evidencia: revisión sistemática y metaanálisis.Aplica a: paciente tras antibioterapia, tabla práctica, mini caso 1 y FAQ sobre utilidad sin colonización persistente.Limitaciones: beneficio dependiente del riesgo basal y de la formulación; no todos los escenarios clínicos son equivalentes. - Goodoory VC, Nguyen L, Passos MC, et al. Efficacy of Probiotics in Irritable Bowel Syndrome: Systematic Review and Meta-analysis. Gastroenterology. 2023;165(5):1206-1218.
doi:10.1053/j.gastro.2023.07.018.
PMID: 37541528.Nivel de evidencia: revisión sistemática y metaanálisis con valoración GRADE.Aplica a: selección de cepas, contexto clínico, síntomas digestivos y mini caso 2.Limitaciones: certeza baja o muy baja en gran parte de los análisis; elevada heterogeneidad entre formulaciones. - Zhang WX, Shi LB, Zhou MS, Wu J, Shi HY. Efficacy of probiotics, prebiotics and synbiotics in irritable bowel syndrome: a systematic review and meta-analysis of randomized, double-blind, placebo-controlled trials. J Med Microbiol. 2023;72(9).
doi:10.1099/jmm.0.001758.
PMID: 37772692.Nivel de evidencia: revisión sistemática y metaanálisis.Aplica a: comparación entre probióticos, prebióticos y simbióticos; sección clínica y controversias.Limitaciones: la evidencia para prebióticos y simbióticos en SII fue incierta por escasez y heterogeneidad de ECA. - Andresen V, Gschossmann J, Layer P. Heat-inactivated Bifidobacterium bifidum MIMBb75 (SYN-HI-001) in the treatment of irritable bowel syndrome: a multicentre, randomised, double-blind, placebo-controlled clinical trial. Lancet Gastroenterol Hepatol. 2020;5(7):658-666.
doi:10.1016/S2468-1253(20)30056-X.
PMID: 32277872.Nivel de evidencia: ensayo clínico aleatorizado multicéntrico.Aplica a: posbióticos/cepas inactivadas, seguridad relativa, utilidad sin viabilidad.Limitaciones: estudio centrado en una formulación concreta y un contexto clínico específico; no extrapolable a todos los posbióticos.
Seguridad
- Merenstein D, Pot B, Leyer G, Ouwehand AC, Preidis GA, et al. Emerging issues in probiotic safety: 2023 perspectives. Gut Microbes. 2023;15(1):2185034.
doi:10.1080/19490976.2023.2185034.
PMID: 36919522.Nivel de evidencia: revisión experta/consenso narrativo.Aplica a: seguridad, calidad, identificación de cepa, grupos vulnerables y checklist final.Limitaciones: no sustituye la evaluación individual del producto ni del huésped; integra evidencia de calidad desigual. - Sotoudegan F, Daniali M, Hassani S, Nikfar S, Abdollahi M. Reappraisal of probiotics’ safety in human. Food Chem Toxicol. 2019;129:22-29.
doi:10.1016/j.fct.2019.04.032.
PMID: 31009735.Nivel de evidencia: revisión narrativa de seguridad.Aplica a: prudencia en inmunocompromiso, pacientes críticos y evaluación beneficio-riesgo.Limitaciones: la calidad de la evidencia de eventos adversos es heterogénea y a menudo procede de series de casos o reportes aislados. - Sanders ME, Akkermans LMA, Haller D, Hammerman C, Heimbach J, Huys G, et al. Safety assessment of probiotics for human use. Gut Microbes. 2010;1(3):164-185.
doi:10.4161/gmic.1.3.12127.
PMID: 21327023.Nivel de evidencia: revisión experta de referencia.Aplica a: marco general de seguridad y evaluación por población diana.Limitaciones: anterior al marco regulatorio y conceptual más reciente; se conserva por su valor fundacional.
Posición de organismos oficiales (guías y consensos)
- Hill C, Guarner F, Reid G, Gibson GR, Merenstein DJ, Pot B, et al. Expert consensus document. The International Scientific Association for Probiotics and Prebiotics consensus statement on the scope and appropriate use of the term probiotic. Nat Rev Gastroenterol Hepatol. 2014;11(8):506-514.
doi:10.1038/nrgastro.2014.66.
PMID: 24912386.Nivel de evidencia: consenso ISAPP.Aplica a: definición de probiótico, necesidad de beneficio demostrado y especificidad del término. - Gibson GR, Hutkins R, Sanders ME, Prescott SL, Reimer RA, Salminen SJ, et al. Expert consensus document: The International Scientific Association for Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of prebiotics. Nat Rev Gastroenterol Hepatol. 2017;14(8):491-502.
doi:10.1038/nrgastro.2017.75.
PMID: 28611480.Nivel de evidencia: consenso ISAPP.Aplica a: definición técnica de prebiótico y uso selectivo por microorganismos del huésped. - Swanson KS, Gibson GR, Hutkins R, Reimer RA, Reid G, Verbeke K, et al. The International Scientific Association for Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of synbiotics. Nat Rev Gastroenterol Hepatol. 2020;17(11):687-701.
doi:10.1038/s41575-020-0344-2.
PMID: 32826966.Nivel de evidencia: consenso ISAPP.Aplica a: distinción entre simbióticos complementarios y sinérgicos. - Salminen S, Collado MC, Endo A, Hill C, Lebeer S, Quigley EMM, et al. The International Scientific Association of Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of postbiotics. Nat Rev Gastroenterol Hepatol. 2021;18(9):649-667.
doi:10.1038/s41575-021-00440-6.
PMID: 33948025.Nivel de evidencia: consenso ISAPP.Aplica a: definición de posbiótico, aclaración de que metabolitos purificados aislados no equivalen automáticamente a un posbiótico. - Guarner F, Sanders ME, Szajewska H, Cohen H, Eliakim R, Herrera-deGuise C, et al. World Gastroenterology Organisation Global Guidelines: Probiotics and Prebiotics. J Clin Gastroenterol. 2024;58(6):533-553.
doi:10.1097/MCG.0000000000002002.
PMID: 38885083.Nivel de evidencia: guía global de organismo científico.Aplica a: uso clínico prudente, relevancia de cepa específica y lectura contextual de la evidencia. - Hutkins R, Walter J, Gibson GR, Bedu-Ferrari C, Scott K, Tancredi DJ, et al. Classifying compounds as prebiotics – scientific perspectives and recommendations. Nat Rev Gastroenterol Hepatol. 2025;22(1):54-70.
doi:10.1038/s41575-024-00981-6.
PMID: 39358591.Nivel de evidencia: recomendación experta.Aplica a: criterios mínimos para clasificar un compuesto como prebiótico y evitar usos laxos del término.
Controversias o límites del conocimiento
- Goodoory VC, Nguyen L, Passos MC, et al. Efficacy of Probiotics in Irritable Bowel Syndrome: Systematic Review and Meta-analysis. Gastroenterology. 2023;165(5):1206-1218.
doi:10.1053/j.gastro.2023.07.018.
PMID: 37541528.Comentario crítico: aunque algunos probióticos o combinaciones pueden ser útiles en SII, la certeza global fue baja o muy baja en gran parte de los análisis por heterogeneidad metodológica y de formulaciones. - Zhang WX, Shi LB, Zhou MS, Wu J, Shi HY. Efficacy of probiotics, prebiotics and synbiotics in irritable bowel syndrome: a systematic review and meta-analysis of randomized, double-blind, placebo-controlled trials. J Med Microbiol. 2023;72(9).
doi:10.1099/jmm.0.001758.
PMID: 37772692.Comentario crítico: la evidencia para prebióticos y simbióticos siguió siendo incierta en SII por número limitado de ECA y variabilidad entre intervenciones. - Merenstein D, Pot B, Leyer G, Ouwehand AC, Preidis GA, et al. Emerging issues in probiotic safety: 2023 perspectives. Gut Microbes. 2023;15(1):2185034.
doi:10.1080/19490976.2023.2185034.
PMID: 36919522.Comentario crítico: la seguridad de los probióticos tradicionales es globalmente favorable en población general, pero la calidad del producto, la verificación independiente y la población diana siguen siendo variables críticas. - Andresen V, Gschossmann J, Layer P. Heat-inactivated Bifidobacterium bifidum MIMBb75 (SYN-HI-001) in the treatment of irritable bowel syndrome: a multicentre, randomised, double-blind, placebo-controlled clinical trial. Lancet Gastroenterol Hepatol. 2020;5(7):658-666.
doi:10.1016/S2468-1253(20)30056-X.
PMID: 32277872.Comentario crítico: apoya que algunos efectos beneficiosos pueden mantenerse sin viabilidad celular, pero no autoriza a extrapolar el concepto a cualquier “posbiótico” o microorganismo inactivado.
¿Quieres saber más?
Echa un vistazo a nuestras formaciones relacionadas con el tema de este artículo: