El eje intestino-articulaciones: microbiota, inflamación y dolor desde la medicina integrativa
En los últimos años, la investigación en microbiota ha ampliado la comprensión de múltiples procesos fisiológicos. Uno de los más relevantes es el eje intestino-articulaciones, un modelo que sugiere que el equilibrio del ecosistema intestinal puede influir en la inflamación sistémica y en la salud del aparato locomotor. Desde la medicina integrativa, este enfoque invita a analizar el dolor articular no solo como un fenómeno mecánico, sino también como una posible manifestación de procesos inmunológicos y metabólicos relacionados con el intestino.
Este cambio de perspectiva está generando nuevas hipótesis clínicas sobre la relación entre microbiota, sistema inmunitario y dolor crónico, especialmente en contextos como la osteoartritis o determinadas enfermedades inflamatorias.
Autor: Redacción ESI
Del modelo fragmentado a la visión integrativa
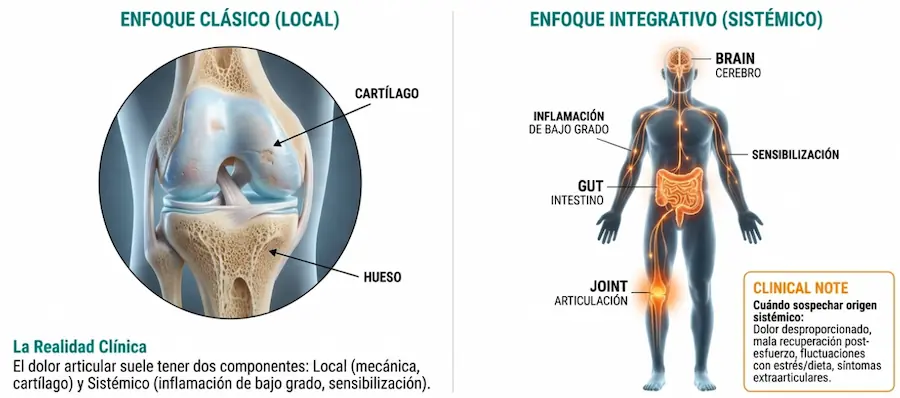
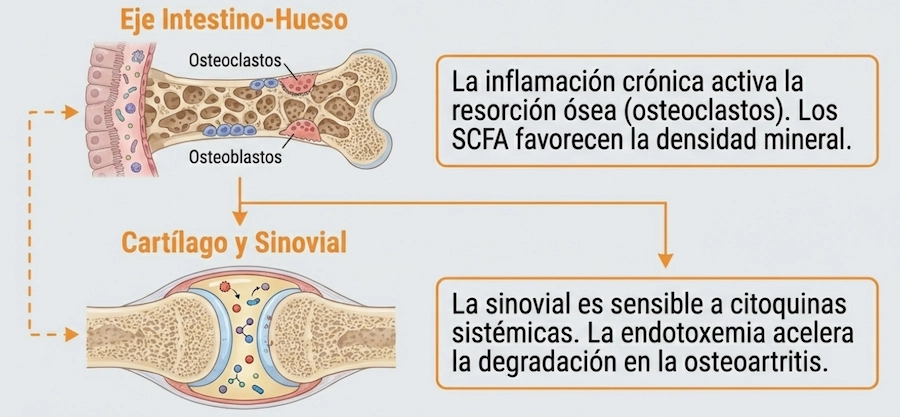
Durante décadas, la práctica médica se ha organizado en especialidades centradas en órganos o sistemas concretos. En el caso del dolor articular, el foco suele situarse en estructuras como el cartílago, el hueso subcondral o la membrana sinovial.
Sin embargo, distintos trabajos de investigación y revisiones científicas han planteado que algunos procesos inflamatorios articulares podrían relacionarse con fenómenos sistémicos, entre ellos alteraciones en la microbiota intestinal o en la regulación inmunológica.
La medicina integrativa propone ampliar el análisis clínico e incorporar elementos como:
- Estado de la microbiota intestinal
- Inflamación sistémica de bajo grado
- Función de la barrera intestinal
- Estilo de vida y estrés crónico
- Nutrición y metabolismo
Este enfoque no sustituye a los abordajes convencionales, pero puede complementar la comprensión de ciertos cuadros clínicos complejos.
La microbiota intestinal y su papel inmunológico
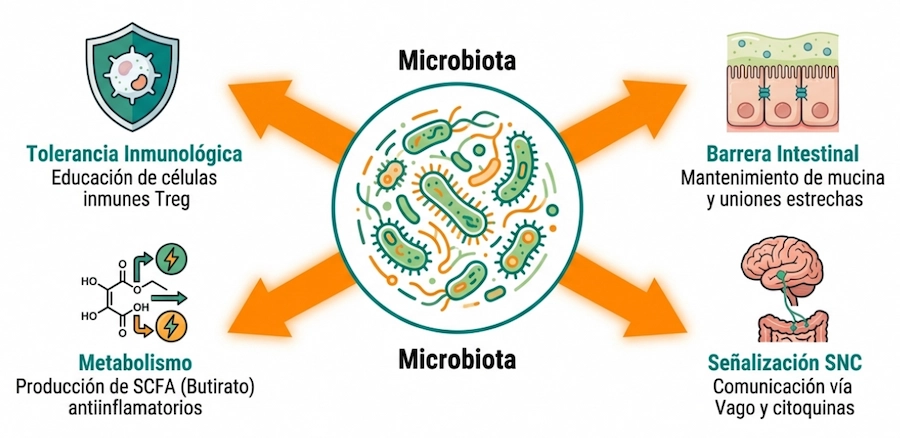
La microbiota intestinal está formada por billones de microorganismos que conviven en el tubo digestivo. Diversas investigaciones sugieren que este ecosistema participa activamente en procesos metabólicos, inmunológicos y neurológicos.
Una de sus funciones más estudiadas es su interacción con el sistema inmunitario. Se estima que una proporción importante de la actividad inmunológica del organismo se encuentra asociada al tejido linfoide intestinal.
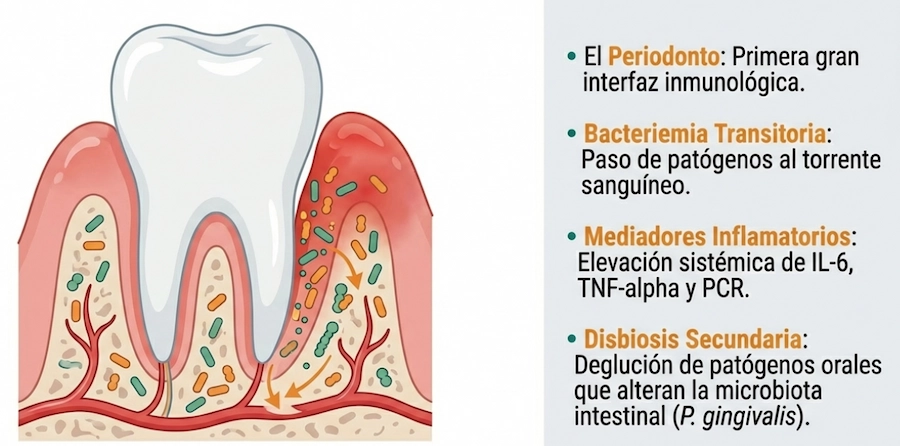
El intestino como interfaz inmunológica
El intestino actúa como un punto de contacto constante entre el organismo y el entorno. A través de la dieta, los microorganismos y diversas moléculas ambientales, el sistema digestivo recibe continuamente señales externas.
Para mantener el equilibrio, el sistema inmunitario intestinal debe desarrollar dos capacidades clave:
- Tolerancia antigénica: reconocimiento de microorganismos beneficiosos sin generar respuesta inflamatoria.
- Regulación dinámica: adaptación continua del sistema inmunitario a los cambios del entorno microbiano.
Cuando este equilibrio se altera, algunos autores describen procesos como disbiosis o alteraciones en la permeabilidad intestinal.
Mecanismos propuestos en el eje intestino-articulaciones
¿Por qué el eje intestino-articulaciones interesa a la investigación actual?
El estudio del eje intestino-articulaciones intenta explicar cómo fenómenos intestinales podrían relacionarse con procesos inflamatorios articulares. Diversas revisiones científicas han propuesto varios mecanismos potenciales.
1. Endotoxemia metabólica
Algunas investigaciones sugieren que determinadas moléculas bacterianas, como los lipopolisacáridos (LPS) presentes en bacterias gram negativas, pueden activar receptores del sistema inmunitario innato.
Cuando estos compuestos alcanzan la circulación sistémica en cantidades relevantes, podrían contribuir a un estado inflamatorio de bajo grado, fenómeno descrito en la literatura como endotoxemia metabólica.
2. Mimetismo molecular
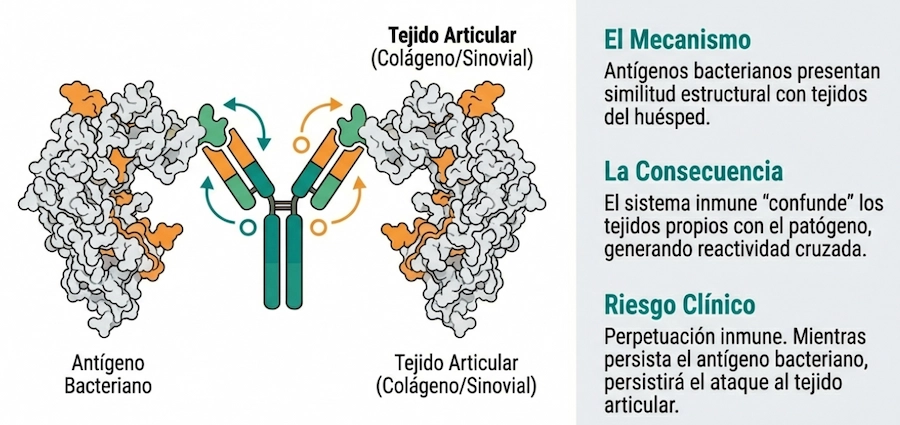
Otro mecanismo propuesto es el mimetismo molecular. En este proceso, componentes de ciertos microorganismos presentan similitudes estructurales con proteínas del propio organismo.
En algunos contextos, esta similitud podría inducir respuestas inmunológicas cruzadas, fenómeno que se ha investigado en diferentes enfermedades autoinmunes.
3. Metabolitos bacterianos
La microbiota intestinal produce metabolitos derivados de la fermentación de fibras dietéticas, como los ácidos grasos de cadena corta (AGCC).
Entre ellos, el butirato ha sido objeto de numerosas investigaciones por su posible papel en:
- Regulación inmunológica
- Integridad de la barrera intestinal
- Modulación de procesos inflamatorios
Una menor diversidad microbiana podría asociarse a una menor producción de estos compuestos.
4. Interacción con el sistema nervioso
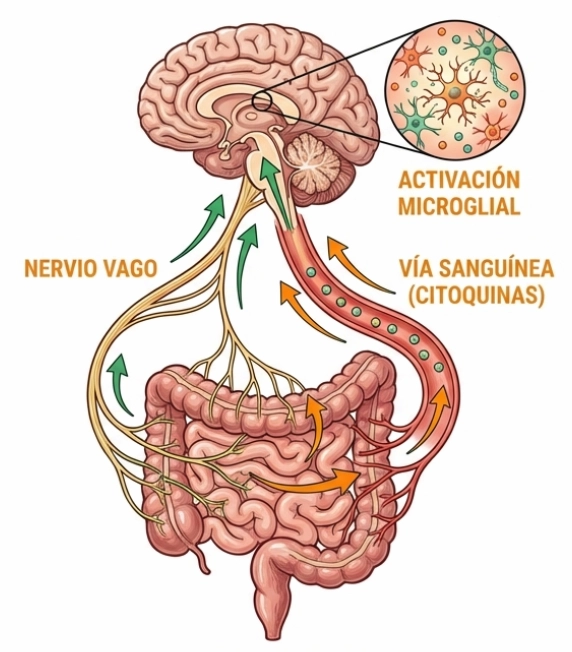
El eje intestino-cerebro describe la comunicación bidireccional entre el sistema digestivo y el sistema nervioso central, mediada por vías nerviosas, inmunológicas y metabólicas.
Algunas investigaciones exploran cómo estas señales podrían influir en la percepción del dolor o en procesos de sensibilización central.
La idea clave
El concepto de eje intestino-articulaciones refleja un cambio progresivo en la forma de comprender los procesos inflamatorios crónicos. En lugar de analizar cada sistema de forma aislada, la investigación actual tiende a considerar redes fisiológicas interconectadas.
En este contexto, la microbiota intestinal emerge como un posible modulador del sistema inmunitario, del metabolismo y de diversos mediadores inflamatorios. Estas interacciones podrían tener implicaciones en tejidos aparentemente alejados del intestino, como el aparato locomotor.
No obstante, es importante subrayar que muchas de estas relaciones se encuentran aún en fase de investigación. Las revisiones científicas disponibles describen asociaciones y mecanismos plausibles, pero la traslación directa a protocolos clínicos requiere una evaluación individualizada y basada en evidencia.
Para los profesionales sanitarios, este paradigma invita a ampliar la mirada clínica: explorar factores dietéticos, intestinales y de estilo de vida que podrían contribuir al contexto inflamatorio general del paciente.
Factores del estilo de vida que influyen en la microbiota
Diferentes variables del estilo de vida pueden influir en la composición y diversidad de la microbiota intestinal.
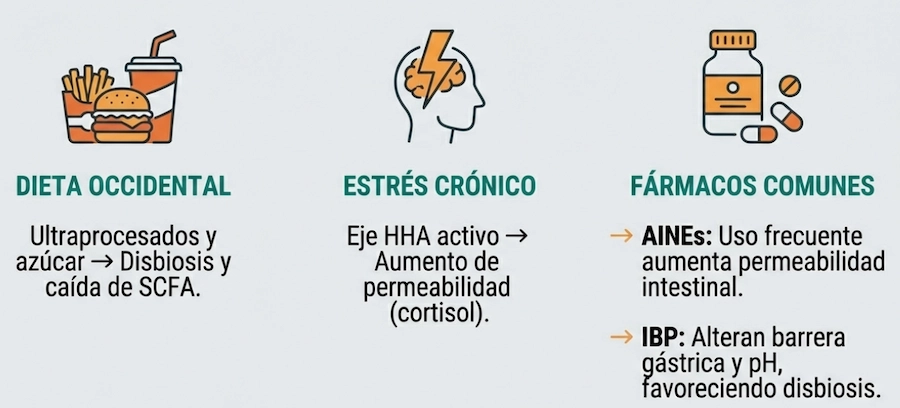
Uso prolongado de ciertos fármacos
Algunos medicamentos pueden modificar el entorno gastrointestinal. Entre los más estudiados se encuentran:
- Antiinflamatorios no esteroideos (AINE)
- Inhibidores de la bomba de protones
- Antibióticos
Las revisiones científicas sugieren que su uso prolongado puede alterar el microbioma intestinal en determinados contextos.
Patrones dietéticos
La alimentación es uno de los factores más influyentes en la composición microbiana intestinal. Dietas pobres en fibra vegetal y ricas en alimentos ultraprocesados pueden reducir la diversidad microbiana.
Por el contrario, patrones dietéticos ricos en vegetales, legumbres y alimentos integrales suelen asociarse con mayor producción de metabolitos beneficiosos.
Estrés crónico
El estrés sostenido puede influir en la función digestiva y en la interacción intestino-cerebro. Diversos estudios exploran cómo la activación prolongada del eje hipotálamo-hipófisis-adrenal podría afectar tanto a la microbiota como a la permeabilidad intestinal.
Cómo aplicarlo mañana en consulta
En la práctica clínica, el modelo del eje intestino-articulaciones puede servir como marco conceptual para ampliar la evaluación del paciente con dolor crónico.
Esto no implica sustituir las herramientas diagnósticas convencionales, sino incorporar preguntas adicionales que ayuden a contextualizar el problema.
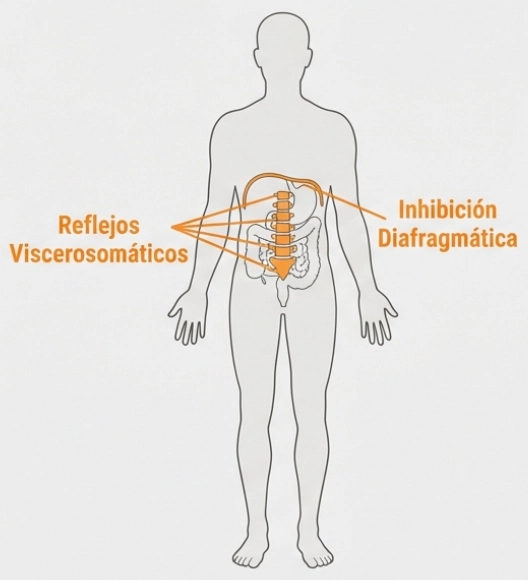
Algunas áreas de exploración clínica incluyen:
- Historia digestiva y síntomas gastrointestinales.
- Patrón dietético habitual.
- Consumo crónico de fármacos gastrointestinales o antiinflamatorios.
- Calidad del sueño y niveles de estrés.
- Nivel de actividad física.
En función del perfil del paciente, el profesional puede valorar intervenciones graduales centradas en nutrición antiinflamatoria, mejora del estilo de vida y apoyo digestivo.
El objetivo no es aplicar protocolos universales, sino identificar factores potencialmente modificables que puedan contribuir al estado inflamatorio global del paciente.
Tabla práctica para la consulta
| Perfil | Hipótesis clínica | Qué priorizar | Señales de mejora |
|---|---|---|---|
| Dolor articular con síntomas digestivos | Alteración de microbiota | Evaluación dietética y digestiva | Mejor digestión y menor rigidez |
| Dolor crónico con fatiga | Inflamación sistémica | Estilo de vida y sueño | Mejor energía diaria |
| Paciente con estrés elevado | Alteración eje intestino-cerebro | Gestión del estrés | Reducción de hipersensibilidad |
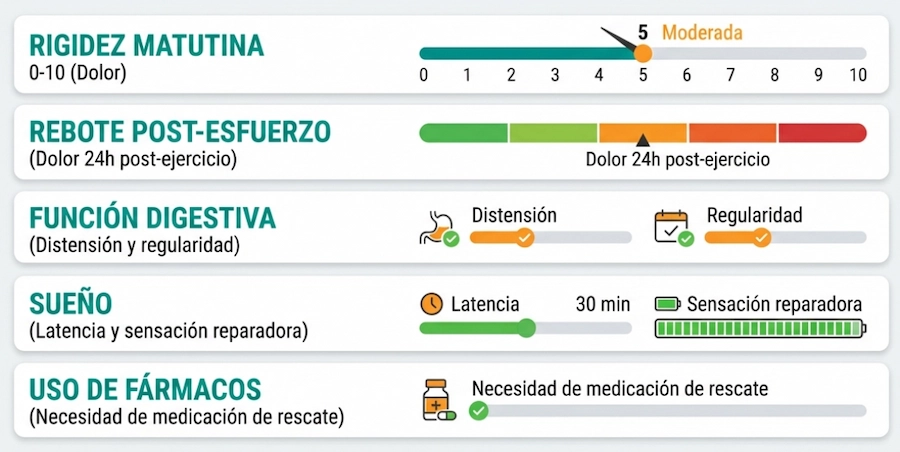
Mini casos clínicos hipotéticos
Caso 1
Paciente de 52 años con dolor crónico de rodilla sin hallazgos radiológicos relevantes. Refiere distensión abdominal frecuente y dieta pobre en fibra. Tras intervención nutricional orientada a mejorar la diversidad dietética, describe mejoría progresiva de síntomas digestivos y percepción subjetiva del dolor.
Caso 2
Paciente con dolor lumbar persistente y alto nivel de estrés laboral. Presenta alteraciones del sueño y síntomas digestivos intermitentes. El abordaje integrativo incluye higiene del sueño, cambios dietéticos y ejercicio moderado.
FAQ sobre el eje intestino-articulaciones
¿Qué es el eje intestino-articulaciones?
Es un modelo fisiológico que estudia cómo la microbiota intestinal y el sistema inmunitario podrían influir en procesos inflamatorios que afectan al aparato locomotor.
¿Puede la microbiota influir en el dolor articular?
Algunas investigaciones sugieren que la microbiota intestinal puede modular procesos inflamatorios sistémicos que podrían relacionarse con la percepción del dolor.
¿La nutrición afecta al eje intestino-articulaciones?
La alimentación influye directamente en la composición de la microbiota intestinal, lo que podría tener implicaciones en procesos metabólicos e inmunológicos.
¿Este enfoque sustituye al tratamiento convencional?
No. El modelo integrativo busca complementar la práctica clínica convencional incorporando factores dietéticos, digestivos y de estilo de vida.
¿Todos los pacientes con dolor articular tienen disbiosis?
No necesariamente. La relación entre microbiota y dolor articular es compleja y todavía se está investigando.
Checklist para profesionales
- Evaluar síntomas digestivos en pacientes con dolor crónico.
- Revisar patrón dietético habitual.
- Explorar consumo prolongado de ciertos fármacos.
- Analizar calidad del sueño.
- Evaluar niveles de estrés.
- Considerar diversidad dietética.
- Promover actividad física regular.
- Valorar contexto inflamatorio general.
- Evitar enfoques reduccionistas.
- Priorizar intervenciones progresivas.
- Integrar educación del paciente.
- Realizar seguimiento clínico.
Referencias bibliográficas
Bibliografía científica
Evidencia mecanística
- Maeda Y, Takeda K. Host–microbiota interactions in rheumatoid arthritis.
Experimental & Molecular Medicine. 2019;51:1–6.
doi:10.1038/s12276-019-0283-6.
(Evidencia mecanística del papel de la microbiota intestinal en la modulación inmunológica y la aparición de inflamación articular; respalda la sección sobre interacción microbiota–sistema inmune). - Şahin N, Salbaş E. The Gut-Joint Connection: Microbiome’s Role in Rheumatic Disease.
Archives of Rheumatology. 2025;40(4):413-421.
doi:10.5152/ArchRheumatol.2025.25192. PMID: 41589431.
(Revisión narrativa sobre el eje intestino-articulaciones y el papel de la disbiosis y la permeabilidad intestinal en inflamación sistémica; respalda el bloque sobre endotoxemia metabólica). :contentReference[oaicite:0]{index=0} - Lu J, Wang Y, Wu J, et al. Linking microbial communities to rheumatoid arthritis: focus on gut, oral microbiome and extracellular vesicles.
Frontiers in Immunology. 2025.
doi:10.3389/fimmu.2025.1503474. PMID: 40308573.
(Revisión sobre mecanismos inmunológicos y mimetismo molecular implicados en enfermedades autoinmunes relacionadas con microbiota). :contentReference[oaicite:1]{index=1} - Wang X, Xu Y, Zha H, Wu J. The gut microbiota-ferroptosis axis: a hypothesis for osteoarthritis pathogenesis and therapeutic implications.
Frontiers in Medicine. 2025.
doi:10.3389/fmed.2024.1412345.
(Hipótesis mecanística que vincula microbiota intestinal, inflamación sistémica y degeneración articular en osteoartritis). :contentReference[oaicite:2]{index=2}
Evidencia clínica
- Maeda Y, Kurakawa T, Umemoto E, et al. Dysbiosis contributes to arthritis development via activation of autoreactive T cells.
Nature. 2016;535(7610):117-121.
doi:10.1038/nature18646.
(Estudio experimental que demuestra la relación entre microbiota intestinal y activación de células inmunes implicadas en artritis). - Chen J, Wright K, Davis JM, et al. An expansion of rare lineage intestinal microbes characterizes rheumatoid arthritis.
Genome Medicine. 2016;8:43.
doi:10.1186/s13073-016-0299-7.
(Estudio clínico que identifica cambios en microbiota intestinal asociados a artritis reumatoide). - Wang DW, Pang XT, Zhang H, et al. Gut microbial dysbiosis in rheumatoid arthritis: a systematic review protocol of case-control studies.
BMJ Open. 2022;12:e052021.
doi:10.1136/bmjopen-2021-052021. PMID: 35365513.
(Revisión sistemática sobre alteraciones de la microbiota intestinal en pacientes con artritis reumatoide). :contentReference[oaicite:3]{index=3} - Zhang X, Zhang D, Jia H, et al. The oral and gut microbiomes are perturbed in rheumatoid arthritis and partly normalized after treatment.
Nature Medicine. 2015;21:895-905.
doi:10.1038/nm.3914.
(Estudio clínico que demuestra alteraciones en microbiota intestinal en pacientes con artritis reumatoide).
Seguridad y limitaciones de la evidencia
- Maeda Y, Takeda K. Host–microbiota interactions in rheumatoid arthritis.
Experimental & Molecular Medicine. 2019;51:1-6.
doi:10.1038/s12276-019-0283-6.
(Señala que gran parte de la evidencia procede de modelos animales y estudios observacionales; la traslación clínica aún es limitada). - Lu J, Wang Y, Wu J, et al. Linking microbial communities to rheumatoid arthritis.
Frontiers in Immunology. 2025.
doi:10.3389/fimmu.2025.1503474.
(Describe heterogeneidad metodológica y dificultad para establecer causalidad directa entre microbiota y enfermedad). :contentReference[oaicite:4]{index=4}
Posición de organismos científicos y revisiones de consenso
- Scher JU, Abramson SB. The microbiome and rheumatoid arthritis.
Nature Reviews Rheumatology. 2019;15:273-284.
doi:10.1038/s41584-019-0203-5.
(Revisión ampliamente citada sobre el papel del microbioma en enfermedades reumatológicas). - Zhuoning T. Multitargeted regulation of rheumatoid arthritis by gut microbiota.
Translational Neuroscience and Systems. 2025.
doi:10.54254/2753-8818/2025.AU26103.
(Revisión reciente sobre intervenciones dirigidas a microbiota y su posible papel en enfermedades articulares). :contentReference[oaicite:5]{index=5}
Controversias o límites del conocimiento
- Sahin N, Salbaş E. The Gut-Joint Connection: Microbiome’s Role in Rheumatic Disease.
Archives of Rheumatology. 2025;40(4):413-421.
doi:10.5152/ArchRheumatol.2025.25192.
(Revisión que subraya que muchos mecanismos propuestos siguen siendo hipotéticos y requieren ensayos clínicos prospectivos). :contentReference[oaicite:6]{index=6} - Wang X, Xu Y, Zha H, Wu J. The gut microbiota-ferroptosis axis in osteoarthritis.
Frontiers in Medicine. 2025.
doi:10.3389/fmed.2024.1412345.
(Evidencia mayoritariamente experimental; la relevancia clínica en humanos aún está en investigación). :contentReference[oaicite:7]{index=7}
¿Quieres saber más?
Echa un vistazo a nuestras formaciones relacionadas con el tema de este artículo: